Las leyes
Ley de las proporciones definidas
Fue enunciado por el químico francés John Dalton en 1804. Esta ley dice:
Diferentes cantidades de un mismo elemento, que se combinan con una cantidad fija de otro elemento para formar diversos compuestos, están en una relación de números enteros y sencillos.
Ejemplo 1:
Para los compuestos formados por la combinación del cloro con el oxígeno tenemos
| Producto | Masa de cloro | Masa de oxígeno |
|---|---|---|
| Cl2O | 2 (35,5) | 1 (16) |
| Cl2O3 | 2 (35,5) | 3 (16) |
| Cl2O5 | 2 (35,5) | 5 (16) |
| Cl2O7 | 2 (35,5) | 7 (16) |
La masa constante es la del cloro, y la masa variable es la del oxígeno.
https://www.fullquimica.com/2014/02/ley-de-proporciones-multiples.html
Ley de las proporciones recíprocas
Fue planteada por J.B. Ritcher y C.F. Wenzel en 1702, quien establece lo siguiente:
las masas de diferentes elementos que se combinan con una misma masa de otro elemento dan la relación en que se combinarán entre sí, o bien múltiplos o submúltiplos de estas masas.
Ejemplo 1:
Sean estas dos reacciones químicas (P.A.: Na=23 , S=32 , H=1)

Ley de los volumenes en combinación
Esta ley establece lo siguiente
A las mismas condiciones de presión y temperatura existe una relación constante y definida de números enteros y sencillos, entre los volúmenes de las sustancias gaseosas que intervienen en unareacción química
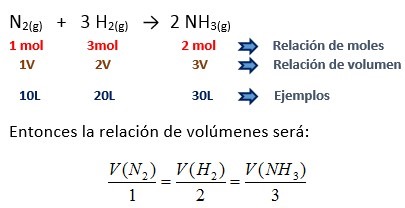
La relación del número de moles (coeficientes estequiométricos) nos indica la relación de volúmenes de las sustancias gaseosas que intervienen en una reacción química, a las mismas condiciones de presión y temperatura.
Ejemplo 1:
Dada la siguiente reacción química: