Querido tú.
Este es un sitio web para que aprecies varios aspectos de un tema con nombre enredado pero finalmente fácil.
Dirígete a novedades
Ahí encontrarás explicaciones.
Es importante que conozcas algunos conceptos básicos
Reacción química
La reacción química es una modificación de los enlaces entre átomos, por desplazamientos de electrones: unos enlaces se rompen y otros se forman, pero los átomos implicados se conservan.
Esto es lo que llamamos la ley de conservación de la materia (masa), que implica las dos leyes siguientes:
1.- la conservación del número de átomos de cada elemento químico
2.- la conservación de la carga total: Las relaciones estequiométricas entre las cantidades de reactivos consumidos y productos formados dependen directamente de estas leyes de conservación, y están determinadas por la ecuación (ajustada) de la reacción.
Ecuación química
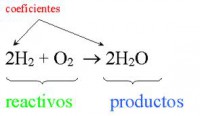
Coeficiente estequiométrico
Es el coeficiente (un número) que le corresponde a cada especie química (elemento) en una ecuación química dada. En el ejemplo anterior:
![]()
Símbolo
Es la representación gráfica de un elemento. El símbolo de un elemento representa no solamente su nombre, sino también un átomo o un número prefijado (“mol”) de átomos de ese elemento.
Fórmula
H es el símbolo químico de un átomo de Hidrogeno; no es una formula.
H2 es la fórmula de dos átomos de Hidrogeno unidos (molécula).
O es el símbolo químico de un átomo de Oxigeno; no es una formula.
O2 es la fórmula molecular del Oxigeno (sustancia simple).
H2O es la fórmula de una molécula de agua (sustancia compuesta).
Peso atómico
En esta página encontrarás algunos conceptos más https://www.eis.uva.es/~qgintro/esteq/tutorial-01.html www.fullquimica.com/2014/02/contraccion-volumetricaestequiometria.html www.fullquimica.com/2014/02/eficiencia-o-porcentaje-de-rendimiento.html


.jpg)